海莉·伯奇发现研究人员如何利用病毒蛋白质来制造新的抗菌药物
在2008年俄罗斯与格鲁吉亚的战争期间,人们曾使用晦涩的疗法来治疗战场上感染的细菌。如果你对噬菌体不太了解的话,那就是晦涩难懂。噬菌体,或称噬菌体,被称为生物圈的“暗物质”。1估计有10个31它们以病毒的形式潜伏在细菌宿主的细胞内。就像病毒接管人类细胞一样,噬菌体接管了细菌的细胞,最终从内部爆炸宿主,释放出微小的后代。正是这种利用细菌破裂蛋白炸毁细菌细胞的能力,使得军方对治疗生病的士兵以及寻找不依赖失效抗生素的新方法来治疗细菌感染感兴趣。
今天,一家位于纽约的公司,ContraFect该公司正努力让噬菌体蛋白被批准用于治疗细菌感染。他们的药物CF-301是一种可以杀死甲氧西林耐药性的酶金黄色葡萄球菌他们希望在人类身上也能起到同样的作用。ContraFect研究副总裁雷蒙德·舒赫解释说,这种酶是在2008年发现的,当时俄罗斯和格鲁吉亚正处于战争状态。但是使用这些类型的酶杀死细菌的想法已经存在了很长时间。
出身卑微
在发现青霉素之前,亚历山大·弗莱明(Alexander Fleming)最初走的是类似的路线。1921年,他在英国伦敦的圣玛丽医院(St. Mary’s Hospital)患重感冒,忙着清理培养皿,在琼脂板上擦拭自己的鼻腔粘液,只是想看看会发生什么。几周后,他注意到分泌物中有杀灭细菌的物质。这是溶菌酶,一种自然产生的抗菌物质,在鼻涕中发现。舒赫说:“它不是来自噬菌体,但它是同一类酶,它能降解目标细菌的细胞。”
噬菌体对抗生素的作用非常不同
虽然酶的想法直到很久以后才开始实施,但基于噬菌体的治疗的第一次人体试验已经进行了。几年前,自学成才的法裔加拿大微生物学家Félix d 'Hérelle从士兵的粪便中提取出整个噬菌体,并用它们治疗儿童痢疾,并取得了一些成功。此后,在20世纪的大部分时间里,波兰、格鲁吉亚和俄罗斯都使用噬菌体鸡尾酒治疗细菌感染。20世纪30年代,格鲁吉亚第比利斯的伊利亚瓦研究所(Eliava Institute)成吨地向苏联军方运送噬菌体。
弗莱明的研究当然改变了历史的进程,他在自己的一个盘子上发现了青霉素,标志着抗生素时代的到来。但波兰20世纪80年代的研究表明,即使在那时,噬菌体疗法偶尔也会在抗生素无法起作用的慢性感染中发挥作用。就这些噬菌体疗法而言,起作用的确切分子可能并不重要,但随着现代生物技术的出现,有可能大量分离、纯化和合成噬菌体衍生分子,从而制造出像CF-301这样的药物。
ContraFect的噬菌体衍生分子是一种内溶酶或溶酶,是一种细菌爆发酶,是目前许多噬菌体蛋白质研究的焦点。在自然界中,噬菌体从内部部署溶酶,利用它们来分解革兰氏阳性细菌坚韧细胞壁中的肽聚糖聚合物,并使它们喷出其内容物——包括由噬菌体制造的新的传染性病毒颗粒。舒赫在洛克菲勒大学的研究小组在猪病原体猪链球菌的基因组中发现了类似溶酶的基因特征。正如舒赫回忆的那样,因为噬菌体将它们的DNA强制进入宿主的基因组以获得控制权,所以这些代码只是“坐在那里”。“我们得到了这个序列,我们克隆了它,表达了它,我们证明了它对链球菌有活性,这很好,但作为一个附带的好处,它对葡萄球菌也有活性。”金黄色葡萄球菌].据舒赫说,在此之前,杀灭葡萄球菌的噬菌体溶菌素被证明很难大量生产。他们已经研究了数百种可能的分子,但最终还是很幸运。
2014年的一项研究2显示克隆酶的表达和产生大肠杆菌-杀死250种不同的金黄色葡萄球菌包括120种耐甲氧西林菌株,比抗生素快得多。它还能清除血液中有葡萄球菌的小鼠体内的MRSA。在健康志愿者的一期试验完成后,针对这种情况的人体试验将于今年开始。与此同时,另一种抗葡萄球菌蛋白,来自噬菌体K,它感染一系列葡萄球菌目前,这家总部位于加州的生物技术公司正在进行临床试验,将其用于鼻腔治疗GangaGen.
杀死的溶菌素
那么,究竟是什么赋予了溶菌素作为抗生素替代品的巨大潜力呢?他们的主要优势是他们的行动方式德维恩罗奇他是法国巴黎巴斯德研究所的研究员,最近写了一篇关于噬菌体蛋白质的综述。“研究来自噬菌体的蛋白质的动力在于,它们不依赖于目前抗生素使用的任何作用模式。它们与抗生素的作用非常不同,这非常有吸引力,因为这样它们就不容易产生细菌已经存在的耐药机制。”
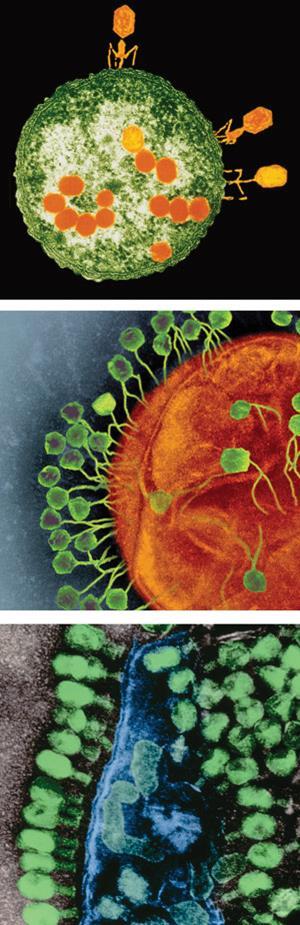
细菌不太可能对噬菌体蛋白质产生耐药性的一个原因是,在治疗方法中,它们的使用方式与噬菌体使用它们的方式不同。不是从内部击破细菌细胞壁,而是将作为药物测试的溶菌素应用于细胞外部。罗奇认为这种“非自然”的攻击方式对细菌来说太陌生了,以至于它们无法对其进行防御。相比之下,大多数抗生素分子都来自于细菌进化来抵御竞争对手的分子,因此它们的工作方式相当容易识别——它们可以进化来逃避。罗奇说,另一个原因很简单,“噬菌体非常擅长成为细菌的捕食者”,所以它们有一些相当无懈可击的方法来做到这一点。
事实上,舒赫实验室的研究结果表明,在达托霉素环境下生长的细菌对达托霉素产生耐药性的速度至少比在CF-301环境下生长的细菌对达托霉素产生耐药性的速度快32倍。在一项较早的关于杀死炭疽杆菌的溶素的研究中,3.舒赫和他的同事无法产生任何耐药细菌,即使他们将培养物暴露在一种已知会导致基因突变的化学物质中。然而,在同样的化学诱变剂的存在下,链霉素的耐药性增加了10,000倍。当然,这并不意味着细菌永远不会对基于溶菌素的药物或任何其他噬菌体蛋白质产生耐药性,但似乎我们在噬菌体产品上比在抗生素上有更多的回旋余地。
结构解决方案
不过还有一些棘手的问题需要克服。首先,内溶素结构很难确定,特别是与细菌细胞壁内的肽聚糖靶标结合时。只有少数内溶素与它们的目标共结晶,或者至少是它们的类似物。如果你能做到的话,他解释道Mark van Raaij他是马德里西班牙国家生物技术中心的结晶学家,你可以从原子的细节上看到蛋白质是如何识别并与细菌结合的。他说:“如果你知道所有这些详细信息,那么你也许可以考虑进行蛋白质工程,使其适应其他肽聚糖,甚至其他菌株或其他细菌种类。”这是我们感兴趣的。
舒赫认为,由于内溶素的模块化结构,它们根本难以结晶。它们由不同的结构域组成,由灵活的连接体连接起来——正是灵活性造成了困难,因为它阻止了稳定晶体的形成。Van Raiij也同意结晶的目的是有问题的,特别是因为并不总是很明显哪些是灵活的部分,但并不比一般的蛋白质更有问题。结晶学家解决这个问题的方法是选择一个结构域,将其单独结晶,然后对另一个结构域重复这一过程,然后将各个部分组合在一起,并尝试预测整个分子的实际样子。
这就是CF-301所采用的方法,而在2014年,Van Raaij的团队明确了这一点4另一种攻击MRSA的溶素的一部分——属于K. Van Raaij正在合作的噬菌体的一部分艾丹科菲以及他在爱尔兰科克理工学院的团队,他们正试图开发一种基于这种分子的抗菌素。他们结晶的区域被称为CHAPK结构域,相当于GangaGen抗葡萄球菌药物的一部分。已知它在两个非常特定的氨基酸之间切割肽聚糖。根据它的结构和其他内溶素的工作原理,他们已经能够对切割过程的反应机制做出有根据的猜测,包括酶活性位点内的三种氨基酸。但要真正了解发生了什么,他们需要共结晶CHAPK与其底物的类似物。范·拉伊吉说:“我们已经尝试了很多,但还没有成功。”如果他们真的成功了,下一个任务可能是决定如何设计这种蛋白质。
设计不同的
罗伯·拉维尼(Rob Lavigne)的团队已经在比利时鲁汶大学(University of Leuven)开始了溶酶蛋白工程。他的研究重点是克服可能是最大的障碍使用溶菌素作为广泛作用的抗菌剂:在自然界中,溶菌素只对革兰氏阳性细菌起作用,而且它们只是问题的一半。许多难以治疗的细菌——比如导致淋病的耐药菌株——都是革兰氏阴性细菌。例如,去年9月,英国公共卫生部(Public Health England)宣布,他们发现了15例高度耐药的淋病,这些淋病对欧洲推荐的标准治疗方法之一大环内酯类抗生素没有反应阿奇霉素.这种药物通常与一种叫做头孢曲松的头孢菌素联合使用。不幸的是,其他欧洲国家已经发现了头孢菌素耐药菌株。
但是为什么溶血素对革兰氏阴性细菌无效呢?因为在这些细菌中,革兰氏阳性菌分子非常擅长分解的肽聚糖细胞壁对它们来说是不可接近的。它被一层外层脂质膜包围着。因此,要穿过外层,要么需要完全不同类型的分子,要么需要首先引导溶菌素穿过内层。艾薇儿的团队选择了后者。他解释说:“我们设计了一种新策略,即穿透外膜,允许内溶素穿过并破坏肽聚糖层。”
他的策略是基于“设计型”内溶素,被称为artilysins,它将普通的溶素与能够破坏革兰氏阴性细胞外膜的抗菌肽结合在一起。这些抗菌肽可以来自任何来源。例如,艾薇儿的团队设计的Art-175分子铜绿假单胞菌,溶酶与绵羊的一种白细胞蛋白偶联。耐药铜绿假单胞菌在医院感染和囊性纤维化患者的慢性肺部感染中是主要问题。试管的初步结果表明Art-175杀死了所有菌株,包括耐多药菌株,5延时显微镜显示细菌细胞在几分钟内就爆炸了。
这个比利时团队与蛋白质研究公司莱山多(Lysando)合作,该公司获得了artilysins的许可,他们希望能解决其他耐药病原体的问题。艾薇儿说:“从理论上讲,针对革兰氏阴性细菌是没有限制的。”“artilysins是一种模块化的方法,通过摆弄这些模块,你可以改变特异性和活性。”“然而,溶菌素的一个关键好处是它们的狭义特异性,这使得它们不会伤害共生细菌或‘好’细菌,例如皮肤或肠道中的细菌。”所以改变它们需要一个谨慎的平衡。
现实的未来
Schuch和ContraFect承认革兰氏阴性是一个重大威胁,他们也在改造溶菌素以应对这些更具挑战性的目标。舒赫非常熟悉这种手工酵素,但他说,他自己的团队也在考虑其他的修改方法,“希望能把它推进一步”。更重要的是,这两个团队都认为,他们的噬菌体疗法可以解决由被称为生物膜的细菌厚斑块引起的慢性感染。这些细菌集体通常存活抗生素治疗,尽管个别细胞明显易感性。
然而,像该领域的其他人(包括艾薇儿)一样,舒赫对关于溶菌素的重大声明持谨慎态度。他更倾向于认为它们不是抗生素的替代品,而是替代品,有可能治疗抗生素正在削弱的许多感染。“从一开始,我们的想法是,它们将进入治疗细菌感染的化学实体套件,所以认为它们将完全取代抗生素,这可能是不现实的。”
的美国食品和药物管理局(FDA)已将CF-301列入快速审批计划,这意味着如果一切顺利,它将成为一流的抗菌素,最初与抗生素联合使用,用于危及生命的病例。罗奇说,该领域的其他人都在期待着会发生什么,然后再加入进来。他说:“有了内溶素,我们正处在人们开始涉足的风口浪尖。”“ContraFect是那些一开始就想做第一的公司之一,但其他公司都想做第二——他们排着队说‘现在它就要发生了,我们将站在它后面’。”
与此同时,一项由欧盟委员会资助的老式噬菌体鸡尾酒试验正在法国、比利时和瑞士的烧伤病房进行。噬菌体,生物圈的“暗物质”,似乎终于得到了人们的关注。
海莉·伯奇是一位生活在英国布里斯托尔的科学作家
参考文献
1M L peddulla等,细胞, 2003,113, 171 (doi:10.1016 / s0092 - 8674 (03) 00233 - 2)
2R Schuch等,j .感染。说。, 2014,209, 1469 (doi:10.1093 / infdis / jit637)
3.R Schuch, D Nelson和V A Fischetti,自然, 2002,418, 884 (doi:10.1038 / nature01026)
4M Sanz-Gaitero等,病毒学, 2014,11, 133 (doi:10.1186 / 1743 - 422 x - 11 - 133)
5Y蒺藜等,Antimicrob。代理Chemother。, 2014,58, 3774 (doi:10.1128 / aac.02668-14)






暂无评论