锂空气电池保持好足够的功率密度燃料汽车的承诺,但近年来他们的进展停滞不前?菲利普发现球
锂空气电池保持好足够的功率密度燃料汽车的承诺,但近年来他们的进展停滞不前?菲利普发现球

你知道这种感觉:当你需要做出至关重要的电话,你的手机电池是平的。但是现在想象你开车穿过偏僻的地方在一个潮湿的夜晚,你还有300英里要走,惊人的电池电量过低的符号闪烁的不是手机,而是你的电动汽车的仪表板。
燃油成本飙升和污染和全球变暖日益恶化,许多人喜欢电动汽车——原则上。但实际上他们是因“里程焦虑”:被困的恐惧没有力量。加满汽油的车里一个家庭可能让你400英里,但是今天的电动汽车很少管理的四分之一,和充电需要时间。所以他们很绝望的长途旅行。
IBM能源技术现在多元化的信息,希望引进电动汽车以其范围问题电池500项目。在2009年推出,它的目标是开发一个电池能够驱动一辆车与一次充电500英里。和许多其他电池研究人员一样,将自己的信念是一个电池可以提高能源的能力超过现有的电池能达到10倍。这电池运行在空气——更确切地说,在精力充沛与锂反应的氧气。氧化锂的低密度,其在理论上可以提供一个能量密度(每公斤)能量释放远高于电池目前常用的电动汽车(主要是镍氢电池和锂离子),和类似的汽油。1
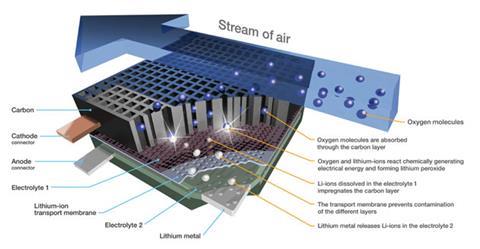
但障碍使锂空气电池车辆令人生畏的实用技术。2它们必须是廉价、安全、可充电和能够承受许多的充放电循环。的安全、范围和成本的关键项目是限制电动汽车的发展,“说电池500项目的经理,“证明IBM的阿尔马登研究实验室在圣何塞,加利福尼亚,主动权。
是复杂的挑战这一事实,尽管原型锂空气电池已经开发出来,但是没有人能完全确定什么是电极的电化学过程,显然这电解质与电极之间的界面是复杂和难以控制。我们需要准确地了解细胞内发生的化学反应,这样他们可以用合适的材料,设计的证明说。这也被证明是件棘手的事情。
空中力量
锂空气电池的首次提出是在1970年代用于电动汽车,但几乎没有严肃的工作发展,直到1996年。当Kuzhikalail亚伯拉罕的研发公司启德实验室在马萨诸塞州诺伍德称,非水可充电设备金属锂阳极,阴极多孔碳和聚合物凝胶电解质。3
使薄和健壮的膜是具有挑战性
在阳极,锂原子失去一个电子形成离子进入电解液含有锂盐的溶解。在阴极,空气,或在这种情况下,和大多数其他设备到目前为止,纯氧-扩散到电极制成导电多孔碳,氧气减少,与锂离子反应生成不溶性锂过氧化,李2O2(见下面的框)。当电池充电时,这种化合物,沉积在碳表面,溶解与锂离子的释放和氧气。在接下来的15年里,这些被认为是电极反应的关键。最近,它已成为明显的故事并非如此简单。
亚伯拉罕“质子”细胞——所谓的因为它使用溶剂,没有轻易ionisable氢离子——仍然是最有前途的设计,但它并不是唯一的。锂空气电池的水电解质也,和有优势,产品在阴极形成可溶性锂化合物(通常氢氧化锂),这可以避免堵塞(见的接口下面的框)。但在这种情况下,锂阳极必须涂上一层屏障,允许锂离子通过,同时保护金属与水反应。除此之外,到目前为止还没有可能使水反应可逆:这些都是一次性的电池,无用的车辆。这就是为什么大多数的焦点目前质子细胞。
材料的差异
在某些方面,质子锂空气电池非常类似于第一个锂电池,锂阳极的也转换为在放电时锂离子。这些被运送非水电解质,如碳酸丙烯酯,阴极由lithium-intercalating材料制成,如锂锰氧化物。所不同的是,空气电池的阴极反应更加精力充沛,产生一个更高的能量密度,而类似的材料。但那些早期的锂电池成为声名狼藉,因为他们倾向于爆炸起火;阳极是容易腐蚀,与电解液反应。在充电周期,金属锂未必是沉积在一个光滑的涂层,但可能成长为分支的手指被称为树突,最终导致设备短路。
锂空气电池面临同样的问题。锂阳极反应溶剂,可能的复杂的有机阴离子锂盐,形成一系列化合物,外套,使钝化表面,防止进一步的反应和创造一个稳定的接口。他们的工作,但它不是很清楚为什么——由此产生的表面是不均匀的,脆弱和化学多样化。
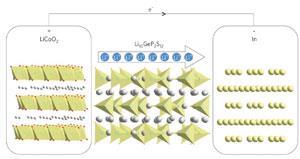
阳极表面的一种方法实现更好的控制一直是上衣与一种保护层,可以传输锂锂离子,如所谓的锂超离子导体陶瓷。去年,丰田的研究人员与东京理工学院的科学家们开发出一种材料,李10《全球经济展望》2年代12非常高的锂离子电导率,并展示其在锂离子电池中使用。4不幸的是,这些陶瓷本身可能容易与锂反应。所以进一步保护薄膜更稳定的锂化合物,如氮化锂或磷化,必须插入电极和厚超离子导体。这是一个相当复杂的界面和制造过程。这防护层的导率一般较低,并使薄,机械地健壮的膜是具有挑战性的,”杰克·克里斯坦森说,一个工程师博世研究和技术中心在帕洛阿尔托,加州。
有很多担心的阴极。这里,锂离子可以意向性还原性与氧发生化学反应,形成各种各样的产品,根据不同的条件——它很可能,例如,锂超氧化物,利奥2,可能会形成以及过氧化。这些不溶性化合物的积累可以抑制反应物到电极表面的流动,他们拿起电子——不仅仅是通过创建一个绝缘涂层的多孔碳表面,但通过堵塞毛孔本身和减少表面积访问。这些问题被认为是一个原因需要充电电池电压高于它产生放电。
潜在的问题
大约五年前,人们发现这种所谓的超电势可以减少阴极表面的催化剂,如金属纳米粒子或氧化物如氧化锰。人们认为这些催化剂的角色之一是加快速度与分子氧降低电极表面。但似乎这所谓的催化作用可能是红鲱鱼。
的论文显示,细胞降低过电压与催化剂如黄金和白金错误地得出结论,所需排放收费的催化反应发生了,”克里斯腾森说。然而,事实证明,这些催化剂只是更有效地将电解液分解。IBM集团已很明确表明,电催化作用在非质子锂空气电池完全没有作用。
虽然彼得·布鲁斯苏格兰圣安德鲁斯大学的同意,催化剂主要是代理的溶剂分解前的工作,他觉得还为时过早排除一个更有用的角色。我们现在才访问电解质和电极有足够稳定来探索这个问题,”他说。
催化剂或没有,电解液的降解是一个严重的问题。在2009年末,一个团队在Susono丰田电池研究部门,日本,发现他们与碳酸丙烯酯电解质锂空气电池是不生产锂氧化物阴极。5研究人员认为,锂离子而不是与电解液反应。
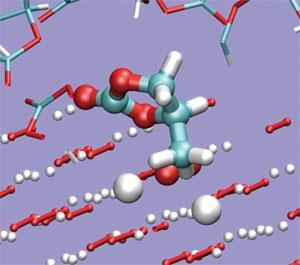
去年,布鲁斯和他的同事们发现,这些反应产生一系列不同的碳酸锂化合物,以及二氧化碳。6今年早些时候,亚历山德罗Curioni和IBM的特奥多罗会苏黎世研究实验室澄清这是如何发生的。他们从头开始反应的分子动力学模拟2O2和碳酸丙烯酯表明过氧化活性固体形式大大超过溶液相单一的单位,烷基carbonate.7碳酸盐分解溶剂
电池吃本身显然是不会走远——这些设备将需要更多的抗氧化电解质。“一旦你知道这背后的类型的化学不稳定,它相对容易屏幕的新溶剂,“Curioni说。这是我们现在做什么。然而,尽管其他溶剂,乙二醇二甲醚、醚等,已经试过了,没有显示完整的可逆性——也就是说,没有副反应,使细胞可以返回在相同的状态,开始收费。我们仍然有不必要的副反应,我们的主要目标是消除这些进一步通过改善电解质,“证明说。
一些研究人员认为离子液体——盐在室温下是液体,它通常包含大型有机离子——可能会提供答案。尽管这些目前已知的也往往是退化的电化学势大,几组是朝着使他们更健壮。溶剂退化的问题也可以减轻通过仔细选择阴极材料。
虽然大多数细胞探索到目前为止使用多孔碳,布鲁斯和他的同事们最近发现,二甲亚砜溶剂的分解可以避免通过使用纳米多孔金阴极。8他们表明,黄金是比二氧化碳更有效促进氧化2O2在充电期间,虽然很为什么——是否它是一种催化,说,还不清楚。金电极将沉重的和昂贵的,但是金色涂布多孔碳也工作得很好。当涉及到成本,布鲁斯指出,有大量的黄金在每一个移动电话。然而,第一个选择是找到一个低成本的选择。”
我们的主要目标是消除不必要的副反应,提高电解质
几乎所有的原型设备制造迄今为止使用纯氧而不是空气,避免不必要的副反应和水蒸气,二氧化碳和氮气。对于任何实际设备,氧气将首先需要提取,或者至少丰富。电池实际上可以使用纯氧在机载坦克——但这介绍了一套全新的约束的经济、基础设施、安全、车辆的重量。证明相信任何实际设备车辆必须使用空气而不是纯氧,虽然克里斯腾森并不排除后者。
水蒸气是一个特殊的问题:它往往总是比氧气更容易通过细胞膜,部分原因是分子小,当然对锂高腐蚀性。即使是疏水性离子液体solvents9不完全排除水。Aishui余上海复旦大学的和他的同事们开发了一种坚实的密封通过混合与疏水疏水离子液体聚合物(聚偏二氟乙烯的共聚物和polyhexafluoropropylene)和疏水(alkyl-coated)二氧化硅微粒。该复合材料允许氧气渗透虽然不含水蒸气,所以设备可以处理环境空气没有金属阳极受到水。10
时间的考验
即使所有这些挑战可以满足,锂空气电池必须可靠地多次充电。目前的原型通常显示显著性能降低后几十充放电周期。Cyclability不施加那么大的需求可能看上去,因为电池500英里范围需要充电只有大约300倍达到一个可观的生命里程150000英里。都是一样的,如果是高度敏感的水分,电池将在真正的车辆不会持续很长时间。
现在一些新电动汽车使用锂离子电池:你的笔记本电脑或移动的大版本。然而,过了大约三十年锂离子电池达到这个阶段,和锂空气电池可能会需要一个类似的时期的研究之前,他们已经准备好去引擎盖下。如果一切顺利,我们会准备好电池用于汽车大约在2025年,“证明说。
这将需要大量的投资。能量储存资金的水平并不能满足必须克服的挑战,”克里斯腾森说。我们需要大大便宜电池,使电动汽车的广泛应用,它将很难得到与传统的锂离子电池。锂空气电池做样子最好的选择,但这将是一个漫长的路程。
菲利普球是一个基于科学作家在伦敦,英国
锂空气电池的电化学
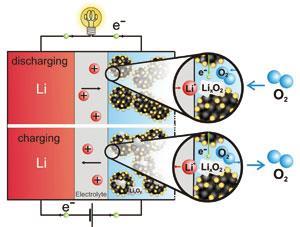
对于一个质子电池(使用有机溶剂),金属锂在阳极氧化:
李?李++ e- - - - - -
在阴极,离子结合分子氧还原过程:
2李++ O2+ 2 e- - - - - -吗?李2O2(年代)
至少,是理论。但在实践中有几个可能的产品锂离子和氧的反应,特别是如果有微量的水或溶剂是不够稳定。和过氧化物可以继续与溶剂反应。
锂空气电池也可以使用水溶剂,在这种情况下,阴极放电反应是:
2李++½O2+ H2O + 2 e- - - - - -吗?2 lioh
这个反应,与非质子的情况下,要求o - o键,乳沟的看来催化剂,如铂、阴极可以是真正有效的。
引用
1 G Girishkumaret al,期刊。化学。列托语,2010,1,2193 (DOI:10.1021 / jz1005384)
2 J·克里斯坦森et al, j . Electrochem。Soc,2012,159年R1 (DOI:jes 10.1149/2.086202)
3 K M亚伯拉罕和Z江,j . Electrochem。Soc,1996,143年,1 (DOI:10.1149/1.1836378)
4 N Kamayaet al, Nat。板牙,2011,10,682 (DOI:10.1038 / nmat3066)
5 F美津浓et al,电化学,2010,78年,403年
6 S Freunbergeret al, j。化学。Soc,2011,133年,8040 (DOI:10.1021 / ja2021747)
7 T会和Curioni化学,2012,18,3510 (DOI:10.1002 / chem.201103057)
8 Z彭et al,科学,2012,337年,563 (DOI:10.1126 / science.1223985)
9 T久et al, j .电源,2005,146年,766 (DOI:10.1016 / j.jpowsour.2005.03.082)
10 D张et al, j .电源,2010,195年,1202 (DOI:10.1016 / j.jpowsour.2009.08.063)









还没有评论