基因移植手术复位藻氢化酶,直接从光系统I捕获电子
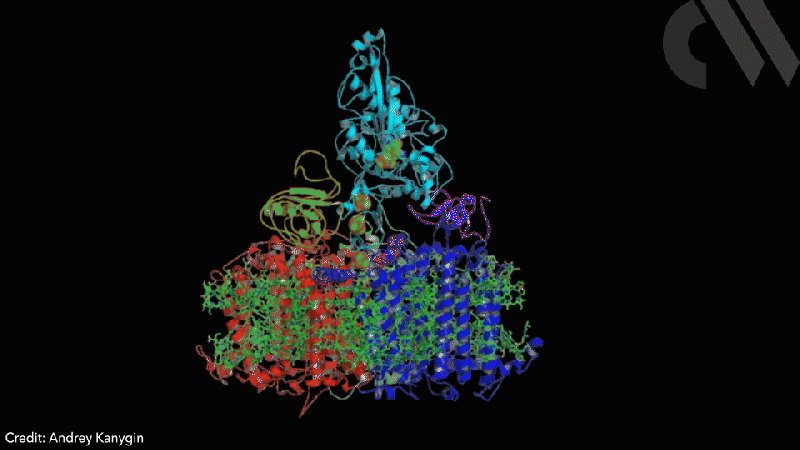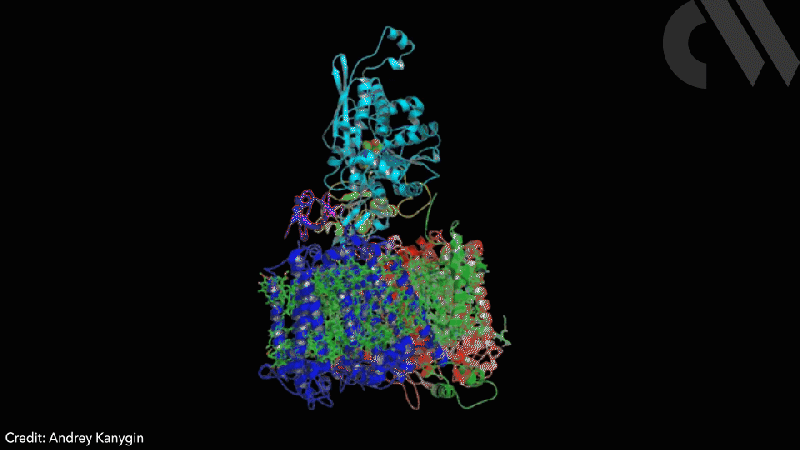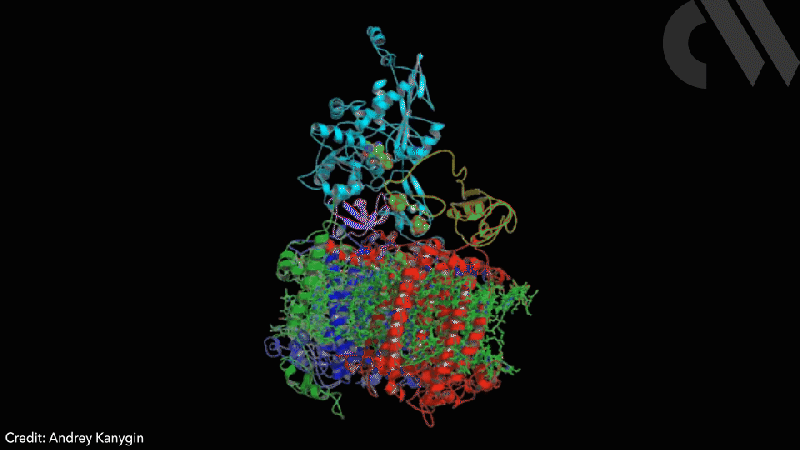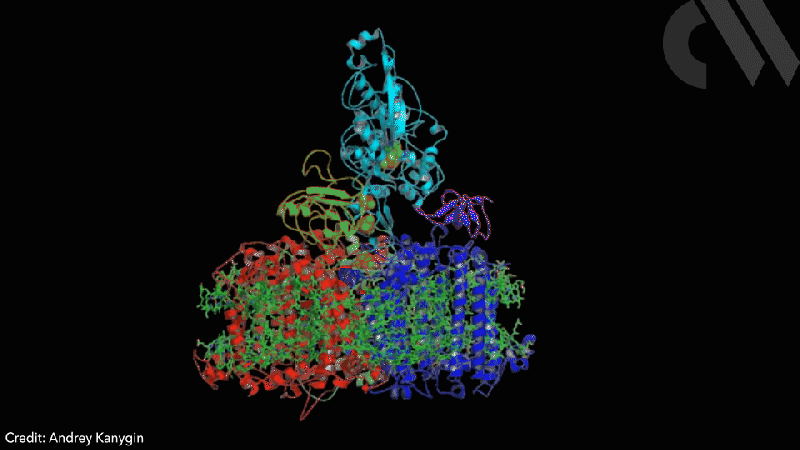
科学家们已经成功地导演光合电子流远离固定二氧化碳和实现减少质子融合在一起光系统I (PSI)和藻氢化酶体内。修改的藻类细胞表达PSI-hydrogenase嵌合体生成氢在高光敏的方式。
而氢是一种很有前途的替代化石燃料,目前95%在美国生产蒸汽甲烷重整,这仍然会产生温室气体。由太阳和使用水作为电子源,在藻类生产氢有潜力成为一个可持续的替代但确实也有自己的挑战。
虽然藻类可以自然产生氢,但产量过低得多的商业可行性。以前曾试图改进过程受到阻碍通过灭活氧氢化酶和细胞内的其他进程争夺电子。
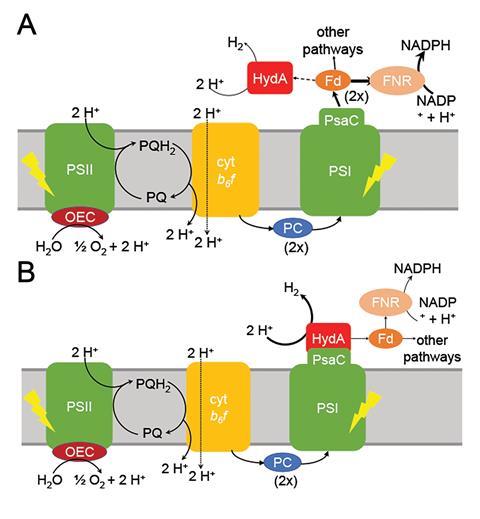
然而,PSI-hydrogenase嵌合体,开发的Iftach Yacoby在以色列,特拉维夫大学凯文·雷丁从亚利桑那州立大学在美国,和他们的同事,克服了电子竞争问题,重新定位藻类的自然氢化酶酶直接捕获电子从光系统I之前进入一般细胞池。我们想出了一种方法,你可以拦截这些电子来自光合作用,在他们的最高能量的地方,这样您就可以驱动有趣的化学反应,”雷丁说。
科学家们花了整个氢化酶的结构基因(hydA2)的绿藻衣藻reinhardtii,通常核基因组中发现,移植到序列PsaC亚基的光系统i他们选定的β-hairpin PsaC氢化酶的最佳插入点,对应于残留32-36 PsaC。那时psaC-hydA2基因引入到叶绿体基因组取代内生psaC基因。这导致修改藻类细胞能产生体内女士每二氢~ 6。
珍妮张专家semi-artificial光合作用在剑桥大学,英国表示,确定该网站在光系统I氧化还原酶可以融合是一个令人兴奋的进步。这无疑将形成未来努力的基础开发藻系统能够有效地执行一系列的太阳能化学形成过程,如二氧化碳转化为有用的原料。这种突破系统的开发仍在很大程度上需要我们的能源生产和二氧化碳回收策略。”
我们现在向试图找到氢化酶的酶更oxygen-resistant,“雷丁说。”希望通过定向进化,我们可能会迫使藻类细胞的氧气,所以,为了生活,他们不得不让氢。”








还没有评论