第一次,铁中形成复杂的经典对硝酸根离子的环测试”被孤立。1背后的团队工作希望解决这个问题困扰了化学家的金属的氧化态半个世纪了。但布朗环化合物原来打破规则,据研究人员介绍,挑战的氧化态的概念定义的国际纯粹与应用化学联合会(Iupac)。

硝酸环测试离子是本科的主要无机分析。浓硫酸和硫酸铁溶液注入试管,样本用于测试添加如果硝酸离子之间存在一个棕色环就会出现酸和硫酸。尽管化学家知道布朗环的化合物,使超过100年,它仍然难以捉摸,没有人能使具体化iron-nitrosyl复杂。
化学家研究不稳定分子在溶液中在铁氧化态分配什么困惑。建议从铁(我)绑定到一个没有+配体,铁(II)与中性甚至没有配体或铁(III)连接到一个没有- - - - - -。
也许问题是我们分类事物的狂热
佩德罗•萨尔瓦多·赫罗纳大学
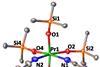
现在,彼得Klufers和Georg Monsch从路德维希马克西米利安慕尼黑大学,德国已经第一个棕色环离子晶体。他们的成功的关键是一个大型酸酯平衡离子perfluoropinacolato配体。棕色环离子是+ 2阳离子,五个水分子和一个亚硝酰配体包围。
然而,他们发现没有提供一个明确的答案的铁的氧化态。相反,它的挑战“氧化态”本身的概念”,作者写道。
根据Iupac氧化态规则,2电子债券被分配到最负电性元素。亚硝酰已经被认为是一个特例,经常给予模棱两可的结果。
来源于一个新的编撰的事情
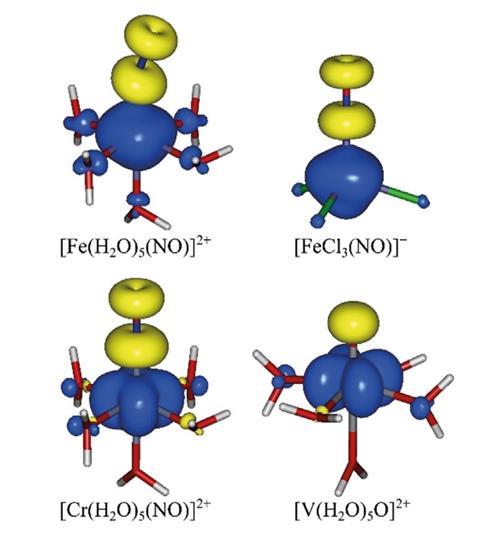
在棕色的发色团,未配对电子和自旋极化使情况变得更加复杂。当他们看着电子属于哪个原子,他们发现自旋向上和自旋向下的电子行为不同。分配给一个原子的自旋向上的电子会旋转到另一个,”解释道佩德罗萨尔瓦多西班牙赫罗纳大学的帮助Klufers和Monsch确定环离子的氧化态。
萨尔瓦多氧化态的有效方法拆解电子分布从轨道计算分配整数氧化态。通常,它提出了相同数量使用路易斯结构作为一个粗略的计算。但布朗环离子不是明确的情况。根据类型的轨道计算Klufers队使用,铁或+ 1 + 3。
棕色的Iupac环的自旋极化使它不兼容的“赢家拿走一切”规则。目前的这种情况下不受规则尽管α-β(旋转)分离是标准的计算方法,在当代的Klufers说。
Iupac已经承认与配体相关的问题像亚硝酰,说约瑟夫Takats来自加拿大阿尔伯塔大学的,他们是团队的一部分,2016年编制的建议。这明确承认有“限制之外,氧化态不再是定义良好的或变得模棱两可的”,这种情况下描述和讨论。Iupac团队的另一个成员,帕特里克•麦卡德尔从爱尔兰高威国立大学补充说,“做分子轨道计算并不是一个好方法了解氧化态”。我们决定使用一个定义基于简单简单的规则可以应用于任何化合物。”
麦卡德尔指出,慕尼黑团队承认,没有强制性的理由反对菲(I)+有利于其他的公式。这是来自定义的公式,”他说。
也许问题是我们对事物分类的狂热,”萨尔瓦多缪斯。而氧化态帮助化学家预测和合理化反应模式,“对一些分子后,我们相信Iupac规则不能得到化学直觉会告诉你”,他补充道。
”(Iupac)任务组他们不关注对模棱两可的情况下计算能做什么,也许他们可以有一点,”萨尔瓦多说。但化学是非常复杂的,很难只有一个规则为我所做的一切。”
引用
1 G Monsch和P Klufers,Angew。化学。,Int. Ed.,2019,DOI:10.1002 / anie.201902374
P 2 P凯伦,麦卡德尔和J Takats,纯粹的达成。化学。,2016,88年,831 (DOI:10.1515 / pac - 2015 - 1204)






1读者的评论