DNA电荷传输从一个酶使移交到另一个地方
DNA携带电子的能力就像一个电线是20多年前发现的。现在,研究人员发现,这种效应可能参与DNA复制,使两个关键酶向另一个发送信号。
我们的模型提出,有快速电子转移通过DNA rna信号之间形成混合DNA引物酶和DNA聚合酶α,”说杰奎琳·巴顿在加州理工学院的,我们。这种“回归”从一个酶的其他启动DNA复制是一个重要的一步。
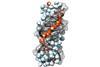
巴顿和她的同事们加入沃尔特Chazin范德比尔特大学的小组,他们一起提出,iron-sulfur集群在DNA引物酶和DNA聚合酶α作为氧化还原“开关”,帮助协调这些酶的分离和绑定到一个DNA链。
巴顿的小组先前表明,电子的转移DNA的氧化态也会影响这些iron-sulfur集群内其他DNA酶参与修复。他们提出的这些酶使用电信号检测DNA损伤。
当Chazin集团发现这些集群复制酶他们决定调查是否类似的机制在起作用。“我们能够显示所需的集群功能,但是不能提出任何合理的解释集群在做什么,”Chazin说。
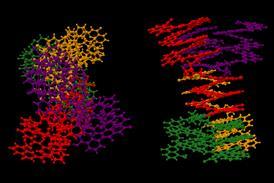
两组DNA介导电化学调查iron-sulfur集群用于DNA引物酶。“我们测量电子转移在金电极修改共价连接双螺旋DNA的电影,”巴顿说。我们可以扫描范围的电压和观察基态之间的电子转移DNA-bound蛋白质和金电极表面,通过其间的双螺旋DNA。
我们发现氧化态(4 fe4s)集群的人类DNA作为可逆氧化还原引发酶功能开关管理DNA结合;氧化(4 fe4s)3 +形式是紧密地绑定到DNA和DNA可以参与电荷转移,而减少[4 fe4s]2 +形式更松散的关联。
团队建议在氧化状态,展开DNA引物酶可以绑定到DNA的复制网站并创建一个互补的RNA引物。当它接收到的电信号,沿着DNA链的DNA聚合酶α就减少,DNA分离,所以其他酶可以取而代之。
这是一个有趣的蛋白质功能和DNA电荷传输之间的联系,”评论杰森溜走达拉斯,德克萨斯大学的我们。未来的努力肯定会探索这种redox-dependent功能的作用在其他形式的DNA复制和DNA修复。”他补充道,“体内的这种效应将巩固断言这项工作的。
Amie Boal,巴顿的前成员的小组现在宾夕法尼亚州立大学,我们说,这个工作真的扩展了我们的知识的可能性的细胞如何利用电荷传输有效地维持基因组的DNA。“在我看来,最有趣的下一步将是理解其他蛋白或通路使用化学和这样不同的系统彼此相交。
引用
E O ' brien等,科学,2017,355年,6327 (DOI:10.1126 / science.aag1789)








还没有评论