随着许多大型制药公司退出中枢神经系统研究,安迪·Extance发现新的药物开发模式正在出现
考虑到谷氨酸是大脑中最常见的神经递质,你如何才能制造出一种药物,使它的副作用最小化?正是这个问题让弗拉德·科里奇(Vlad Coric)走上了成为BioHaven Pharmaceutical首席执行官的道路,当时他正在附近的耶鲁大学(Yale University)学习医学。科里奇回忆说:“我发现,当我们给人们服用氯胺酮时,是的,通过调节谷氨酸,你可以获得抗抑郁和其他治疗效果。”然而,他担心,反复使用氯胺酮被认为会使人有出现类似精神病症状的风险,从而限制其治疗作用。
尽管存在这种担忧,但近年来,一种氯胺酮是少数几种获得市场批准的针对大脑的药物之一。长期以来,氯胺酮一直被用作麻醉剂,现在,氯胺酮的两种镜像对映体形式的活性版本被提纯和销售,使其成为一种获得专利的抗抑郁药成为可能。由此产生的分子艾氯胺酮,现在由美国跨国公司强生(Johnson & Johnson)的制药子公司杨森(Janssen)以鼻腔喷雾剂Spravato的形式销售。然而,它并没有被普遍接受。例如,2020年1月,英国国家健康和护理卓越研究所(Nice)发布了指南草案,反对推荐使用它。
杨森英国治疗区医疗事务主任蒂托·罗奇亚指出,尼斯的评估过程正在进行中。他说:“当然,我们对最初的结果感到失望,但我们仍然决心确保患有难治性重度抑郁症的患者能够获得一种重要的新治疗选择。”“艾氯胺酮鼻喷雾剂提供了30年来治疗重度抑郁症的首个新机制。我们致力于在接下来的评估过程中解决尼斯的问题。”
这个具体的问题是在普遍缺乏针对大脑目标的候选药物的背景下出现的。大型制药公司长期以来一直在缩减他们的中枢神经系统(CNS)研发项目。Janssen是一个明显的例外,该公司研究了22种用于神经精神病学和神经退行性疾病的潜在新药,其中3种处于中后期开发阶段。然而,从2009年到2014年,大型制药公司的中枢神经系统药物发现和开发项目下降了52%,几乎所有公司都出现了下降。1尽管在精神健康和其他中枢神经系统疾病方面仍有大量需求未得到满足,但这种情况仍在继续。
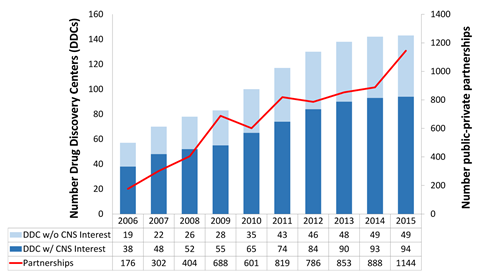
Roccia强调,精神疾病和神经疾病的研究和开发是出了名的具有挑战性。他说,在该地区的临床试验中,招募和留住患者的问题很常见,这导致了额外的成本和延误。其他研究人员认为,药物审批过程并不适合中枢神经系统药物的开发。与此同时,大脑的复杂性以及由此产生的理解难度是许多大型制药公司退出这一领域的根本原因。但是,大学研究中心和较小的公司正在介入,经常与大型制药公司合作。通过这样做,他们开始了重建针对大脑的治疗管道的漫长过程。
超越单一受体
毫无疑问,制药行业已经被开发治疗阿尔茨海默病的新药的长期、昂贵和不成功的斗争所拖延。他们的方法通常依赖于药物来减少β-淀粉样蛋白的产生,这种蛋白会在患者的大脑中形成粘性斑块。澳大利亚悉尼大学的药物化学家Michael Kassiou指出,它们未能产生令人信服的益处。他说,这是因为我们对中枢神经系统生物学还不够了解。他说:“我们依赖于临床前动物模型,这些模型不能完全概括人类病理。”“当淀粉样蛋白小鼠模型产生时,人们认为‘我们将治愈阿尔茨海默病’。我们所做的是治愈了成千上万只痴呆老鼠,但在临床中什么都没有得到转化。”
这部分归因于以谷氨酸盐为代表的中枢神经系统复杂性,其中一种物质具有多种作用。在神经元之间的信号传递中,谷氨酸与至少四种不同类型的受体蛋白相互作用。相比之下,传统的小分子药物发现通常只优化一种类型的蛋白质靶点。Kassiou说,这在药物研发过程中非常常见,以至于监管机构希望测试能够分析单一药物与单一靶标的相互作用。卡苏说:“这行不通。”“我们需要从多方面来看待中枢神经系统疾病。你对疾病生物学有了广泛的了解,需要开发出能够与这些途径相互作用的药物。”
同样,近年来研究的重点是将潜在药物的结构与靶蛋白进行匹配。Kassiou也主张远离这种情况。2他说:“开发真正能够改善疾病的药物的方法是一种表型方法。”研究表型包括观察生物体中可观察到的变化。例如,美国加利福尼亚州的索尔克生物研究所已经开发出了研究神经细胞是否死亡的筛选试验。3.这可能有助于开发与老年神经退行性疾病或中风有关的药物。“你说,‘我从治疗中得到了预期的反应吗?,然后回过头来,找出一个或多个实际目标是什么,这些目标可能是我们没有考虑到的。Kassiou指出,这种方法的吞吐量并不高。然而,他认为与多靶点方法相结合,它们提供了“开发真正有效疗法的最佳机会”。
药物开发软件和服务公司Certara正在推广用于中枢神经系统药物开发的定量系统药理学(QSP),作为解决大脑复杂性的另一种方法。Certara位于英国坎特伯雷的QSP负责人Piet van der Graaf说:“通常,药物发现项目集中在单一的生物物理尺度上。”然而,他解释说,研究模型经常忽略不同尺度上过程之间的联系。4QSP结合了不同的生物物理尺度,将分子发现扩大到“认知过程的水平”,范德格拉夫说。他解释说,它定量评估了对治疗的反应机制。Certara正积极应用QSP来更好地了解脑部疾病的作用机制。它还承诺为评估药物效果和优化临床试验设计提供“更准确、更全面的方法”。
让更多玩家参与进来
在分子尺度上,van der Graaf帮助整合了药代动力学和药效学(PK/PD)建模与代谢组学,以研究多巴胺拮抗剂remoxipride。除了在Certara的工作,他还是荷兰莱顿大学的系统药理学教授。莱顿大学的研究小组将PK/PD建模与通过超高高效液相色谱结合串联质谱(UPLC-MS/MS)测量的remoxipride在大鼠体内分解成代谢物的数据联系起来。5范德格拉夫说:“血浆和大脑药物暴露情况由药代动力学决定,以驱动潜在的多个靶点的结合和激活。”代谢组学可以评估下游的生化效应,这“强调了生物标志物在中枢神经系统药物开发中的重要性和潜力”。
van der Graaf说,为了更好地理解药理作用,需要收集这类生物标记物的多个水平的数据。他说:“最终,这些生物标志物将与临床开发期间的生理指标和临床结果联系起来。”van der Graaf总结说,成功将需要在许多情况下进行详细的生物标志物评估,“并通过在多个物种中应用多种中枢神经系统药物来产生原理证明”。
神经科学家Barbara Slusher说,这种复杂性意味着中枢神经系统药物的开发时间明显长于其他治疗领域。她是美国巴尔的摩约翰霍普金斯大学药物研发项目的主任,她说这促使许多大型制药公司采取“风险分担策略”。斯拉舍解释说:“他们更多地采用一种开放的创新模式,让制药、生物技术和学术界通力合作。”“大多数针对中枢神经系统的早期药物发现和开发都是在小型、有针对性的生物制药公司进行的。其中很多都是从学术发现中衍生出来的。她指出,来自风险投资家的资金正越来越多地用于学术药物研发工作。他说,我认为大型制药公司会让这一概念得到验证,然后参与进来,利用他们的大型开发引擎来推进项目。
Slusher在约翰霍普金斯大学领导着一个专门的药物研发团队。像她这样的团队可以与中枢神经系统专家合作,这些专家“经常在单一疾病领域或治疗目标上花费一生的研究时间”。她说,在制药业很少有这样深入的专业知识。制药公司和风险资本家也认识到了这一点,为针对新靶标的药物研发提供资金。她解释说:“如果成功了,那么大学和制药公司或风险投资集团就会成立一家新公司,并推动它向前发展。”
选择正确的目标
约翰霍普金斯大学的几个阿尔茨海默氏症内部项目研究的目标不仅仅是降低β-淀粉样蛋白水平。这家药物研发集团还向制药公司授权了新型中枢神经系统药物,尽管他们不能透露这些药物是什么。其中一个合作伙伴是日本制药公司卫材(Eisai),约翰霍普金斯大学与该公司有长期合作关系。Slusher和她的同事们确定了新的药物靶点,并与制药公司分享。如果Eisai对靶标感兴趣,约翰霍普金斯大学的研究人员开发了一种高通量筛选试验。与卫材的科学家合作,他们可以测试制药公司的大量潜在药物分子中是否有任何有前途的药物。斯拉舍解释说:“当我们对这些热门药物进行发现时,如果我们发现了什么,公司拥有优先使用权。”“我们的一个CNS靶标通过了这种高通量筛选,然后被授权给卫材。”
Roccia指出,伙伴关系和合作是杨森致力于解决具有挑战性的医疗条件的关键,在这些条件下,需求仍未得到满足。通过他们,公司可以“利用世界上最好的科学专业知识,这使我们能够更有效地运作,为我们的患者带来利益”。失眠和相关的重度抑郁症患者就有这样一种未被满足的需求。詹森正在与Minerva神经科学公司共同开发一种名为seltorexant的药物来治疗这种疾病。它针对的是一个在20世纪90年代末才被发现的大脑系统,涉及神经肽食欲素。罗奇亚解释说:“大脑中的促食欲素系统参与控制几个关键功能,包括新陈代谢、应激反应和清醒状态。”Seltorexant是一种食欲素-2受体拮抗剂,其有效性尚未得到三期临床试验的证实,他补充道。
与此同时,BioHaven制药公司证明了小型、有针对性的生物制药公司可以发挥的作用。Coric强调,其偏头痛治疗药物rimegepant (Nurtec)于2020年2月获得美国食品和药物管理局(fda)批准,这表明当大脑生物学得到充分理解时,一切都是可能的。他解释说,降钙素基因相关肽(CGRP)的水平与偏头痛发病率升高有关,已经有四种药物阻断CGRP受体并缓解偏头痛。但它们都是单克隆抗体,必须在医院使用。因此,BioHaven开发了一种小分子药物,人们可以在家服用。
寻找风险较小的策略
现在,BioHaven正在寻求针对谷氨酸盐的类似成功。过量饮酒是有害的,包括运动神经元疾病、强迫症和阿尔茨海默氏症。但它是我们大脑中最丰富的兴奋性神经递质,是正常功能所必需的,科里奇解释道。他警告说:“它是一种非常重要的神经递质,不能抑制或增加它——在两个极端都有问题。”因此,BioHaven开发了一种治疗方法,以提高位于大脑神经胶质细胞上的转运蛋白水平。科里奇说:“它像吸尘器一样吸收谷氨酸,将其带入神经胶质,将其转化为谷氨酰胺,它就不再具有神经毒性了。”同样的运输过程也将谷氨酰胺反馈到谷氨酸生产中,保持谷氨酸水平稳定。科里奇说:“增加骑行次数,如果谷氨酸盐过高,就会降低。”“如果温度太低,它就会升高,就像恒温器一样。“一种名叫利鲁唑的药物已经在肌萎缩性侧索硬化症(也称为运动神经元疾病)中发挥了这一作用。 But in pill form it’s absorbed so poorly from people’s guts it requires long fasting periods.
因此,BioHaven已经探索了300种可能的利鲁唑前药版本,经过特别修改,使人们更容易从肠道中吸收它。一旦这些前药中最好的三曲鲁唑进入血液,酶就会把它分解成利鲁唑,从而增加谷氨酸转运体的水平。BioHaven目前正在对三曲鲁唑进行2-3期临床试验,用于治疗阿尔茨海默氏症、强迫症和退行性遗传疾病脊髓小脑性共济失调(SCA)。科里奇将这种方法称为“一篮子试验方法”,并建议将其作为成功开发针对大脑的药物的策略。他说:“我们记录了大约10种不同的疾病,可以进行研究,无论是临床前还是临床,都有充分的证据表明谷氨酸在其中发挥了作用,现在对每种疾病都有同样的投入。”“这与阿尔茨海默病和β-淀粉样蛋白症相反,在这两种病中,每个人都全力以赴,如果你输了,15年的时间和数十亿美元就会化为乌有。”
Slusher强调,这样的失败表明需要更多的基础科学。她补充说,认识到这一点将导致中枢神经系统药物的“药物发现模式的重大变化”。这些模式现在可能正在从像她这样的集团和以小公司为目标的制药巨头中蔓延开来。但斯拉舍说,这在短期内可能不会很明显。她强调:“这是20年、30年的时间,不是短期的。”
安迪·Extance是英国埃克塞特的自由科学作家
参考文献
1 B·H·约克利,M·哈特曼,B·S·斯拉什,ACS化学。>, 2017,8, 429 (doi:10.1021 / acschemneuro.7b00040)
2 J J Danon, T A Reekie, M Kassiou,化学发展趋势, 2019,1, 612 (doi:10.1016 / j.trechm.2019.04.009)
3米先验等,ACS化学。>, 2014,5, 503 (doi:10.1021 / cn500051h)
4 H海尔茨等,CPT药物计量系统。杂志, 2020,9, 5 (doi:10.1002 / psp4.12478)
5 W J van den Brink等,欧元。j .制药。Sci, 2017,109, 431 (doi:10.1016 / j.ejps.2017.08.031)







![支柱[6]MaxQ的化学结构](https://d2cbg94ubxgsnp.cloudfront.net/Pictures/100x67/6/2/1/523621_chempr1747_proof1_891632.jpg)



暂无评论