获奖背后的科学基因编辑工具,可以改变我们的生活
Emmanuelle贝纳和詹妮弗Doudna挖了2020年诺贝尔化学奖”发展的基因组编辑的方法。具体地说,他们被授予奖发现Crispr-Cas9基因组编辑技术,允许科学家做出精确改变生物体的遗传密码。Crispr-Cas9是一个功能强大的工具,它可以彻底改变我们的生活的许多方面,从医疗到我们生产食物的方式。这也是近年来看到其公平份额的争议。在这里,我们来看一个更深的这些“基因剪刀”,为什么他们获得了诺贝尔奖。
为什么它赢了吗?
因为贝纳和Doudna开始调查Crispr-Cas9系统在2011年,该领域已经爆炸了。由于相对简单和Crispr系统的负担能力,世界各地的研究人员已经能够运用各种不同的问题的工具。今天有整个期刊、会议和企业致力于技术。
能够减少任何DNA分子选择站点有巨大的潜在治疗遗传疾病——从创建抗病作物。试验还表明Crispr-delivered基因改造可以在人群中的传播疟疾感染的蚊子和停止——这种“gene-drives”提供了一种完全消灭这种疾病。在面对Covid-19大流行,研究人员发现方法在冠状病毒快速诊断测试和使用Crispr也提出了用它来攻击病毒的基因组。
诺贝尔委员会主席,克拉斯Gustafsson化学,在颁奖声明说,“这个基因是巨大的力量的工具,它会影响我们所有人。”
Crispr甚至被用来制造技术更美味的啤酒。
它是如何工作的呢?
整个Crispr基因编辑工具已被改编自细菌的免疫系统。Crispr一词来自集群定期中间短回文的重复序列,指不同的基因序列中发现的细菌的基因组。每个Crispr序列转录成RNA序列,将针对病毒的DNA。这些序列还包括中科院(Crispr-associated)为DNA-cutting ca酶基因代码。导游RNA和ca酶组合在一起形成了一个复杂的狩猎病毒DNA和排骨。
这个系统在Crispr基因编辑,科学家们重新设计指南RNA的大约20个碱基序列匹配一个DNA序列他们希望目标细胞的基因组中。这搭配Cas9酶RNA序列,将DNA链的目标网站。整个的DNA序列编码这两个组件Crispr-Cas9工具可以通过质粒传递到靶细胞。
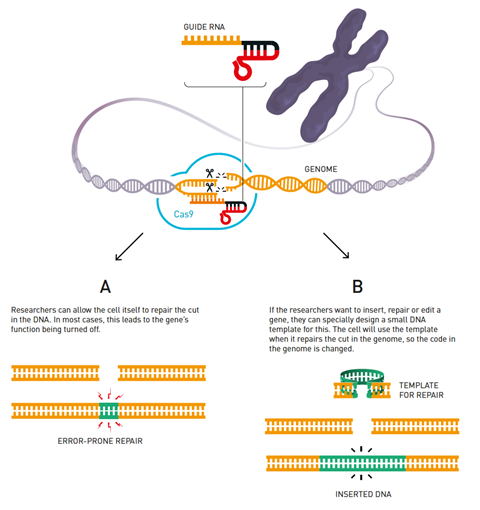
因此可以使用该工具来编辑一个细胞的基因组以难以置信的精确度——例如,它可以剪下一个功能失调的基因与遗传相关疾病。如果健康版本的基因也交付给细胞,细胞的修复系统将把健康链在网站裂解。
获奖者做了什么呢?
2011年,当调查的细菌酿脓链球菌贝纳发现,分子称为tracrRNA形式Crispr-Cas系统的关键部分细菌。
与此同时,Doudna被调查的功能中科院基因,了解到Cas蛋白质编码参与切割DNA的一部分细菌免疫系统抵抗致病病毒。

那一年贝联手Doudna进一步调查系统。他们一起揭示了Cas9蛋白质,CrisprRNA和tracrRNA一起剪DNA链分为两部分。然后简化系统通过结合CrisprRNA tracrRNA成单分子——指导RNA,使其更容易使用,并显示如何可以用来减少任何DNA链在他们选择的一个网站,打开大门使用该工具在各种各样的基因组编辑实验。
虽然以前的遗传工具编辑Crispr-Cas9之前就已经存在,更简单、更便宜的新工具。这导致了田野的大幅扩张,使基因编辑访问所有世界各地的科学家。
所以争议在哪里?
多年来Crispr一直的中心旷日持久的专利纠纷。Doudna和贝纳的发现后不久,冯张的团队广泛研究所的剑桥,专利在真核细胞中使用技术的方法。有Doudna之间旷日持久的法庭斗争在加州大学伯克利分校的集团,我们,和广泛的团队拥有知识产权的关键部分。与此同时,众多组织和公司已获得许多新的Crispr-related技术专利,这意味着随着时间的推移,原专利争端的中心变得不那么重要。
另一个领域的争议围绕使用基因组编辑工具的潜在后果。随着基因组是如此复杂,我们不能总是知道会发生什么当我们编辑的基因。一些基因有多个,常常未知函数——编辑他们纠正一个问题可能会创建新的不可预见的问题。这是特别重要的在编辑时生殖细胞(那些可以传递给生物体的孩子),因为修改后的基因可以遗传给下一代。
作为一种相对较新的技术,我们也知道Crispr本身并不完美。一些研究表明削减非标靶,该工具在额外的位置剪断DNA链所需的网站。这显然可以产生有害的后果,因此,许多研究人员正在寻找方法来提高技术,使它更适合医学使用。
考虑到这些问题,全世界的科学家——包括Doudna和贝纳呼吁暂停在编辑人类生殖系细胞,直到我们可以知道更多关于后果。这样的呼吁愈演愈烈流氓后,中国科学家他Jiankui编辑人类胚胎,然后带到2018年任期。他现在是判了三年徒刑进行这项研究。
接下来会发生什么?
几个临床试验已经开始Crispr-based疗法,承诺报告今年新兴。今年2月,第一项研究观察癌症治疗使用Crispr-edited免疫细胞的报道修改后的细胞是安全的三个病人,没有严重的副作用。而在癌症治疗的疗效是最小的,它可能帮助告知未来Crispr-based t细胞治疗。
一个月后,患者的遗传性失明成为第一个人Crispr-Cas9疗法直接注射到身体。在6月,瑞士基因编辑公司Crispr疗法宣布两个β地中海贫血患者和一个与镰状细胞病将不再需要输血后骨髓干细胞使用Crispr技术编辑。
本周早些时候,Doudna推出了一个新公司,文士疗法,在治疗肌萎缩性脊髓侧索硬化症开始工作。
其他Crispr-based技术接近商业现实。例如,美国基因组工程公司eGenesis开发使用的技术编辑猪的基因,这样他们的器官可能将安全地移植到人类。在农业领域,许多公司正在研究如何使用Crispr加快农作物的选择过程和可取的特征,如抗病或改进的味道。
在基本层面上,研究人员正在研究如何改善系统本身。通过使用替代Cas蛋白质,有些团体希望使工具更有效和更容易使用在某些设置。Doudna集团最近报道在CasX蛋白小于Cas9,可能更容易引入到靶细胞。
额外的信息
提供DNA在细胞和组织是基因治疗的一个重要组成部分,Crispr-Cas9方法更是如此,因为质粒携带这个系统是非常大的。本研究论文描述一个病毒性向量提供质粒DNA携带Crispr-Cas9进入肿瘤球状体,这是很好的体外模型组织也挑战使转染的目标。
1 S J Zamolo T Darbre J-L Reymond,使转染组织模型与CRISPR / Cas9质粒DNA使用多肽树枝状分子,化学。Commun。,2020,DOI:10.1039 / d0cc04750c
调节Crispr-Cas9的功能是议程上的许多研究人员因为能力限制它在空间和时间的方式打开门来精确操纵基因和最小化任何副作用。通过引入对光不稳的团体进入系统,这些研究人员已经表明他们可以调节Cas9活动与光
2 Y王等,Photocontrol CRISPR / Cas9函数定位指导RNA的化学改性化学。科学。,2020,DOI:10.1039 / d0sc04343e
看来Crispr-Cas系统不只是方便基因编辑。本文描述了Crispr-Cas系统被用来组装一个包含五个不同酶的饲料级联。背后的团队的工作希望可以开始构建复杂的一种通用方法,搭建biocatalytic通路
3 S Lim等CRISPR / Cas-directed可编程的组装工艺等的复合体,化学。Commun。,2020,56,4950 (DOI:10.1039 / d0cc01174f)
圆的东西,这里有一些评论Crispr-Cas9是如何工作的,治疗纳米颗粒和交付过程的生理障碍的过程
4 Y徐、刘R和Z戴,关键因素设计CRISPR / Cas9-carrying纳米颗粒治疗基因组编辑,纳米级,2020,DOI:10.1039 / d0nr05452f
5 Y龚等、脂质和聚合物介导CRISPR / Cas9基因编辑,j .板牙。化学。B,2020,8,4369 (DOI:10.1039 / d0tb00207k)










还没有评论